

Copyright©生策會.生策中心 本文內容受著作權法保護,如有引用,請註明出處
2023年是臺灣生醫產品研發(藥品、醫材)國際授權豐收的一年,共有11項產品(藥品10項、醫材1項)推進國際授權,相較2022年增加5項,而已揭露授權金額(含研發里程金)上看超過15.36億美元,超過2022年的3.3億美元。
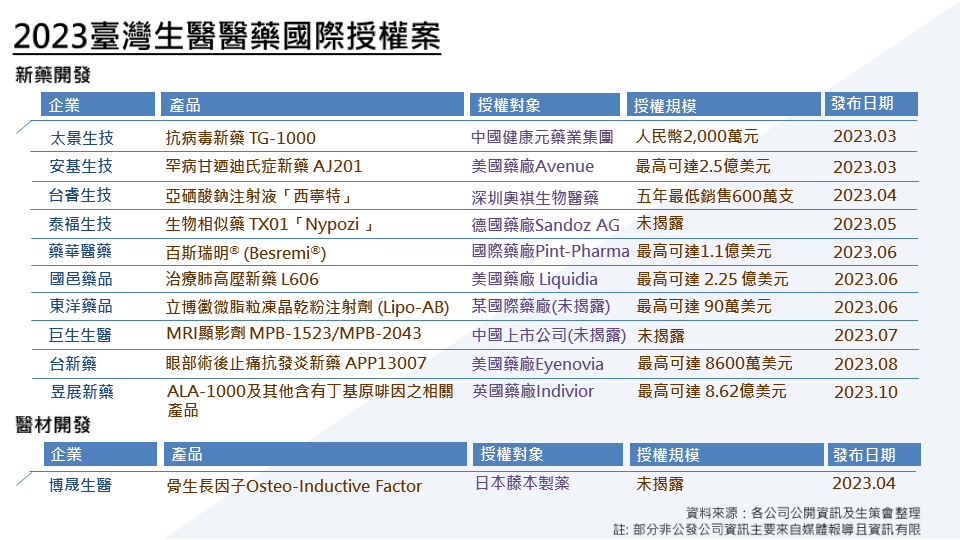
*本文針對新藥開發超過5000萬美元之大型授權案件與醫材授權案件的授權藥物、授權時開發進度、授權規模等,彙整2023年臺灣生醫產品研發國際授權成果。
新藥5件大型授權案 昱展8.62億美元金額最高
臺灣生技新藥研發歷經20多年發展,近年陸續進入開花結果階段。在臺灣生技製藥公司多元發展之下,除了常見的學名藥、小分子藥物及大分子藥物(生物製劑)開發外,改良型新藥(505(b)(2))開發成果也相當豐碩,吸引國際藥廠授權。
總覽年度新藥授權中,5件新藥開發大型授權案(總金額超過5000萬美金),共有3件屬於505(b)(2)新藥以及大分子、小分子新藥各1件,分別為:昱展新藥生技的ALA-1000(8.62億美元)、安基生技新藥的AJ201(2.5億美元)、國邑藥品科技的L606(2.25億美元)、藥華醫藥的百斯瑞明®(1.1億美元),以及台新藥的APP13007(8,600萬美元)。
新藥開發前五大國際授權案件(依授權規模排序)
昱展新藥旗下的長效型治療鴉片類成癮症注射劑ALA-1000(1、3、6月長效劑型)以及其他含有丁基原啡因(Buprenorphine)的相關產品,在2023年10月與全球戒毒藥龍頭Indivior PLC公司簽署全球(臺中港澳除外)授權合約,簽約金達1,500萬美元(約新台幣4.7億元),首項授權產品有權獲得最高達5,500萬美元(約新台幣17.2億元)的研發里程碑金,以及其他產品最高達4,200萬美元(約新台幣13.1億元)研發里程碑金。
待產品上市後,自每項產品年度淨銷售額超過1億美元開始,昱展能獲得總額最高可達7.5億美元(約新台幣236.3億元)銷售里程碑金,合計里程碑金最高可達8.62億美元(約新台幣271.6億元),以及依銷售額級距,獲得10%~15%的銷售分潤。
安基生技新藥
◾ 授權藥物名:AJ201
◾ 授權對象:美國上市新藥公司Avenue Therapeutics
◾ 藥物分類:小分子新藥
◾ 授權時藥物開發進度:完成臨床I期
◾ 授權規模:最高可達2.5億美元
安基生技新藥開發針對罕病甘迺迪氏症的AJ201,在2023年3月與美國那斯達克上市生技新藥公司Avenue Therapeutics Inc.簽署歐美(涵蓋美國、加拿大、歐盟、英國和以色列)專屬授權合約,簽約金達300萬美元(約新台幣9,400萬元)以及後續里程碑金,最高可達2.5億美元(約新台幣75億元),並能獲得百分比兩位數(實際數字未揭露)的銷售分潤。
國邑藥品科技
◾ 授權藥物名:L606
◾ 授權對象:美國藥廠Liquidia
◾ 藥物分類:505(b)(2)新藥
◾ 授權時藥物開發進度:進行臨床III期中
◾ 授權規模:最高可達2.25億美元
國邑藥品開發針對治療第一類肺動脈高壓(PAH)及第三類間質性肺病相關肺高壓(PH-ILD)的L606,在2023年6月與美國藥廠Liquidia Technologies Inc.簽署授權北美合約。根據合約,Liquidia將依照後續試驗進度、藥證申請等支付里程碑金,合計最高可達2.25億美元(約新台幣70億元)。未來取證上市後,國邑將負責藥品的生產、充填。
藥華醫藥
◾ 授權藥物名:Besremi®(百斯瑞明®)
◾ 授權對象: 國際藥廠Pint-Pharma
◾ 藥物分類:大分子新藥 (生物製劑,BLA)
◾ 授權時藥物開發進度:取得多國藥證
◾ 授權規模:最高可達1.1億美元
繼09年授權奧地利AOP Orphan Pharmaceuticals AG後,藥華醫藥旗下治療真性紅血球增多症(PV)的新藥Besremi®(百斯瑞明®),在2023年6月與國際藥廠Pint-Pharma GmbH簽署拉丁美洲7國(涵蓋阿根廷、巴西、智利、哥倫比亞、厄瓜多、墨西哥、秘魯)商業授權合約。根據合約,由Pint按照時程進行Besremi®的藥證申請與商化銷售,並支付藥華藥里程碑金,總金額最高可達到1.1億美元(約新台幣34.48億元),以及藥品上市後雙位數百分比的銷售權利金。
台新藥
◾ 授權藥物名:APP13007
◾ 授權對象:美國上市製藥公司Eyenovia
◾ 藥物分類:505(b)(2)新藥
◾ 授權時藥物開發進度:完成臨床III期
◾ 授權規模:8,600萬美元
台新藥繼2021年將旗下針對眼部術後止痛抗發炎新藥APP13007的中國與港澳市場授權給遠大醫藥後(授權金額900萬美元),在2023年8月與美國上市製藥公司Eyenovia, Inc.簽署美國市場獨家授權合約。
根據合約,台新藥將獲得簽約金、發展里程金及銷售里程金,合計最高8,600萬美元(約新台幣27.5億元)。 並且台新藥已於2024年3月4日接獲美國FDA通知,APP13007通過新藥申請審查,預計2024年年中展開銷售,由台新藥負責供貨、Eyenovia負責後續美國市場銷售。
醫材授權加速國產醫材取證與商化效率,博晟與國際夥伴共創雙贏!
醫材開發國際授權案件
博晟生醫旗下研發中骨再生產品 - 骨生長因子(Osteo-Inductive Factor, OIF)在2023年4月與日本Fujimoto Pharmaceutical(藤本製薬株式会社)簽署日本獨家授權合約,授權金額未揭露。
根據合約內容,將由Fujimoto Pharmaceutical負責OIF在日本執行的後續臨床試驗及取證上市的全額費用,博晟將可大幅減少研發支出,並可共享臨床試驗數據資料;待產品上市銷售後,可收取雙位數的銷售分潤。

